Ion sulfat, sunfat hay sulfate là một Ion với công thức hóa học SO²⁻ ₄. Các muối, các phân nhánh axit, và các peroxide sunfat được dùng rộng rãi trong công nghiệp. Các muối sunfat tồn tại rộng rãi trong tự nhiên. Sunfat là các muối của axit sulfuric và hàng loạt muối này được điều chế trực tiếp từ axit trên. Vậy nhóm SO4 hóa trị mấy và Công thức kim loại M với nhóm SO4 ra sao, mời các bạn cùng tìm hiểu dưới bài viết này.

SO4 hóa trị mấy?
– Hóa trị của nhóm =SO4 là II
Công thức: SO₄²- Khối lượng phân tử: 96,06 g/mol Phân loại: Hợp chất vô cơ Có thể hòa tan trong: Nước Công thức phân tử: SO2−; 4
Công thức kim loại M với nhóm SO4
Hợp chất của kim loại M với nhóm SO4 có công thức là M2SO4
Photpho ( P ) hóa trị mấy? ứng dụng và tính chất của P
Silic ( Si ) hóa trị mấy? Tính chất hóa học và ứng dụng của Silic
Nhôm hóa trị mấy? kí hiệu và nguyên tử khối của Al
Ví dụ :
Hợp chất của kim loại M với nhóm SO4 có công thức là M2SO4.PTK : 342 Tính toán để xác định M là nguyên tố nào
Lời giải :
Phân tử khối của M2(SO4)3 :342g/mol
=> 2M+3 x (32 + 4 x 6 ) = 342
=> M = ?
Tra bảng 1 SGK/42g thì ta có tên và ký hiệu hóa học của nguyên tố M.
Muối sunfat. Nhận biết ion sunfat
1. Muối sunfat
Muối sunfat là muối của axir sunfuric. Có 2 loại muối sunfat:
– Muối trung hoà (muối sunfat) chứa ion sunfat SO42-. Phần lớn muối sunfat đều tan trừ BaSO4, SrSO4, PbSO4 không tan.
– Muối axit (muối hiđrosunfat) chứa ion hiđrosunfat HSO4-
2. Nhận biết ion sunfat
Thuốc thử nhận biết ion sunfat SO42- là dung dịch muối bari. Sản phẩm phản ứng là bari sunfat BaSO4 kết tủa trắng, không tan trong axit.
– Cách nhận biết muối sunfat
H2SO4 + BaCl2 →BaSO4 + 2HCl
Na2SO4 + Ba(OH)2 →BaSO4 + 2NaOH
Axit sunfuric
1. Tính chất vật lý
– Axit sunfuric (H2SO4) là chất lỏng sánh như dầu, không màu, không bay hơi, nặng gần gấp 2 lần nước (H2SO4 98% có D = 1,84 g/cm3).
– H2SO4 tan vô hạn trong nước và toả nhiệt rất nhiều nhiệt. Nếu ta rót nước vào H2SO4, nước sôi đột ngột và kéo theo những giọt axit bắn ra xung quanh gây nguy hiểm. Vì vậy, muốn pha loãng axit H2SO4 đặc, người ta phải rót từ từ axit vào nước và khuấy nhẹ bằng đũa thuỷ tinh mà không được làm ngược lại.
Ứng dụng
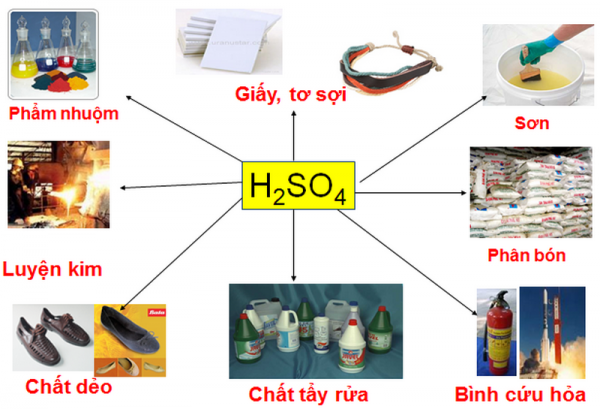
– Axit sunfuric là hoá chất hàng đầu được dùng trong nhiều ngành sản xuất. Hàng năm, các nước trên thế giới sản xuất khoảng 160 triệu tấn H2SO4.
– Axit sunfuric được dùng để sản xuất phân bón, thuốc trừ sâu, chất giặt rửa tổng hợp, tơ sợi hoá học, chất dẻo, sơn màu, phẩm nhuộm, dược phẩm, chế biến dầu mỏ…
Xem thêm bảng hóa trị và hóa trị của các nguyên tố:
Bảng Hóa Trị Lớp 8, Cách Học Thuộc Bằng Bài Ca Hóa Trị Hóa Học.
Bạc ( Ag ) hóa trị mấy? Cấu tạo của nguyên tử và tính chất của Ag
NO3 hóa trị mấy? Cấu tạo phân tử NO3 chuẩn
Lưu huỳnh ( S ) có mấy hóa trị, nguyên tử khối của S
