1. Công thức hóa học của đường Saccharose
1.1. Công thức hóa học của đường Saccharose là gì?
Saccharose được biết nhiều với nhiều cái tên quen thuộc như đường kính (độ tinh khiết của đường cao), đường cát, đường ăn, đường trắng, đường nâu (đường có chứa tạp chất màu), đường mía (đường sinh ra từ trong thân cây mía), đường phèn (tồn tại ở dạng kết tinh), đường củ cải (đường chứa trong củ cải đường), đường thốt nốt (đường chứa trong cây thốt nốt) hay một cách đơn giản ngắn gọn là đường.
Sucroza, saccarozo hay saccharose là một disaccarit (kết hợp giữa glucose và fructose). Tên hóa học của đường ăn là α-D-glucopyranosyl-(1→2)-β-D-fructofuranozit (kết thúc bằng “ozit” vì bản chất của nó không phải là đường khử). Nó được sử dụng phổ biến vì vai trò của nó trong khẩu phần ăn uống của con người và vì nó được hình thành bên trong thực vật chứ không phải từ các loài sinh vật khác.
-
Công thức hóa học của đường mía là C12H22O11
-
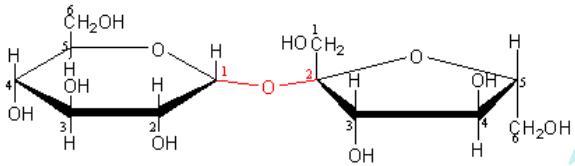
Nếu như cả fructozo và glucozo đều được gọi là monosaccarit thì đường saccharose lại được gọi là disaccarit, vì cấu trúc của saccharose là dạng mạch vòng và được liên kết bằng 1,2-glycozit nên gốc α-glucozo sẽ kết hợp cùng β-fructozo
-
Saccharose thường được biết đến nhiều hơn với cái tên là đường mía vì loại đường này có rất nhiều bên trong mía
-
Saccharose sẽ bị thủy phân tạo ra fructozo và glucozo trong môi trường axit là vì saccharose không chứa nhóm OH hemiaxetal
Một số thông tin khác:
• Khối lượng của phân tử là 342,3 g/mol
• Điểm nóng chảy của đường là 186°C
• Khối lượng mol của đường là 342.29648 g/mol
• Độ hòa tan trong nước của đường là 211,5 g/100 ml (20°C)
• Khối lượng riêng của đường là 1,587 g/cm3
1.2. Tính chất hóa học của đường Saccharose
Vì không chứa nhóm chức andehit (-CH=O) nên saccharose không có tính khử như ở glucozo (không xảy ra phản ứng tráng bạc). Đường saccharose có mang tính chất của ancol đa chức và đường này cũng có phản ứng của đisaccarit.
a) Đường có tính chất của ancol đa chức
Dung dịch saccharose hòa tan được kết tủa Cu(OH)2 thành một loại dung dịch phức đồng – trong đó saccharose có màu xanh lam
2C12H22O11 + Cu(OH)2 → (C12H21O11)2Cu + 2H2O
b) Phản ứng của đisaccarit (hay còn gọi là phản ứng thủy phân)
Saccarozơ khi xảy ra phản ứng thủy sẽ hình thành nên glucozơ và fructozơ khi:
+ Được đun nóng với dung dịch axit
+ Có sự tham gia xúc tác của enzym trong hệ tiêu hóa của người
C12H22O11 + H2O -(H+,to) → C6H12O6 + C6H12O6
Saccharose Glucozo Fructozo
– Saccharose khi nóng chảy và phân hủy với nhiệt độ là 186°C sẽ tạo ra caramen (hay còn gọi là đường thắng).
– Đường saccharose khi cháy sẽ hình thành ra carbon, CO2 và H2O. Nước có khả năng phá vỡ cấu trúc của saccharose nhờ xảy ra phản ứng thủy phân nhưng quá trình thực hiện diễn ra rất chậm. Chính vì thế mà saccharose có khả năng tồn tại trong dung dịch trong rất nhiều năm mà gần như không có sự thay đổi về đặc điểm tính chất. Tuy nhiên, nếu phản ứng có thêm xúc tác của enzym sucrazo thì phản ứng sẽ xảy ra một cách nhanh chóng.
– Saccharose bị phân hủy trong môi trường có sự tham gia xúc tác của axit sunfuric đậm đặc và tạo thành carbon.
C12H22O11 → 12 C + 11 H2O (có xúc tác của H2SO4 đặc)
2. Công thức hóa học của đường Mantozo
2.1. Công thức hóa học của đường Mantozo là gì?
Mantozo còn được gọi là đường mạch nha, là một phần chủ yếu của nhiều loại thực phẩm và đồ uống quen thuộc thường ngày. Đường được sản xuất trong quá trình malting tạo ra bia và rượu mạch nha, cũng như trong quy trình lên men cần thiết để làm ra bánh mì hoặc bánh mì tròn. Ở trạng thái thô, hầu như những loại thực phẩm đều chứa mantozo cho đến khi chúng trở thành màu nâu hoặc caramen. Nó cũng được hình thành bởi thực vật khi hạt của chúng bắt đầu vào quá trình nảy mầm và bởi ruột của con người khi chúng ta tiêu thụ tinh bột.
Trong số những đồng phân của saccarozơ, đồng phân quan trọng nhất là mantozơ (hay còn gọi là đường mạch nha).

– Ở trạng thái tinh thể thì phân tử mantozơ bao gồm hai gốc glucozơ liên kết với nhau ở vị trí C1 của gốc α-glucozơ này với vị trí C4 của gốc α-glucozơ kia quan một nguyên tử oxy. Liên kết α có dạng là C1-O-C4 nên gọi là liên kết α-1,4-glicozit
– Trong dung dịch, gốc α-glucozơ của đường mantozơ có khả năng mở vòng và làm xuất hiện nhóm CH=O
2.2. Tính chất hóa học của đường Mantozo
Vì cấu trúc như trên đường mantozơ có 3 tính chất chính như sau:
a) Tính chất của poliol giống saccarozơ:
– Có khả năng tác dụng với Cu(OH)2 cho ra phức đồng-mantozơ màu xanh lam.
2 C12H22O11 + Cu(OH)2 → (C12H21O11)2Cu + 2 H2O
b) Tính khử của Mantozơ cũng giống như tính khử của glucozơ
– Khử [Ag(NH3)2]OH tạo ra kết tủa bạc (đây chính là phản ứng tráng gương với dd AgNO3 trong NH3)
C12H22O11 + 2 AgNO3 + 2 NH3 + H2O → 2 Ag + NH4NO3 + C12H22O11
– Tác dụng với Cu(OH)2 hình thành kết tủa màu Cu2O dưới điều kiện đun nóng.
c) Phản ứng thủy phân
– Phản ứng thủy phân khi có mặt của xúc tác axit hoặc xúc tác enzym sẽ tạo ra 2 phân tử glucozơ.
C12H22O11 + H2O → 2 C6H12O6
– Mantozơ được điều chế bằng phản ứng thủy phân tinh bột nhờ vào enzym amilaza (thành phần có trong mầm lúa). Phản ứng này cũng xảy ra bên trong cơ thể của người và động vật.
Tham khảo ngay bộ tài liệu tổng hợp kiến thức và phương pháp giải mọi dạng bài tập thi THPT Quốc Gia môn Hóa ngay

3. Công thức hóa học của đường Glucose
3.1. Công thức hóa học của đường Glucose là gì?
Đường glucose là một thành phần chủ yếu có trong đường và nhiều loại gia vị quen thuộc khác trong tất cả các bữa ăn hằng ngày của mọi gia đình. Ngoài ra chúng cũng chiếm hàm lượng lớn trong một số thực phẩm như hoa quả, tinh bột,… Đáng chú ý hơn, Glucose còn được biết đến là thành phần dinh dưỡng dự trữ, cung cấp nguồn năng lượng cho toàn bộ cơ thể và có vai trò tham gia vào cấu trúc của tế bào nên còn có tên khác là đường máu, đường huyết.
-
Đường Glucose tồn tại dưới 2 dạng là dạng mạch vòng hay dạng mạch hở (mạch thẳng), 2 dạng mạch này thường hay có sự chuyển hóa qua lại với nhau nhờ vào phản ứng của các nhóm chức nằm trong phân tử: nhóm -OH và nhóm -CHO sẽ tự xảy ra phản ứng với nhau, mạch vòng được tạo ra từ các nhóm này là 1 vòng gồm có 6 cạnh, với đỉnh của vòng đó chính là nguyên tử O
-
Glucose hay còn có một cái tên khác thường gọi là đường nho, loại đường này thường có nhiều trong các loại hoa quả, nhất là trong quả nho.
-
Công thức hóa học của đường glucose CH2OH – CHOH – CHOH – CHOH – CHOH -CH=O được viết rút gọn là CH2OH [CHOH] 4CHO => CT phân tử của đường là C6H12O6

-
Các nhóm OH còn lại có vị trí phân bố thích hợp với sự tối ưu hóa về mặt không gian, thích hợp với điều kiện tồn tại của hợp chất này.
-
Nhóm OH ở vị trí C1 được gán màu sắc có tên là nhóm OH hemiaxetal, nhóm này thể hiện được những đặc trưng riêng biệt chỉ có trong tính chất của đường glucose.
Một số thông tin khác về đường glucose
• Khối lượng mol của đường glucose là 180.16 g/mol
• Khối lượng riêng của đường glucose là 1.54 g/cm3
• Điểm nóng chảy của của đường glucose: a-D-glucose là 146°C, B-D-glucose là 150°C
• Độ hòa tan trong nước của đường glucose là 91 g/100 ml (điều kiện nhiệt độ 25°C)
3.2. Tính chất hóa học của đường mía – đường Glucose
Glucose mang các tính chất của anđehit (do cấu trúc phân tử có chứa nhóm chức anđehit -CHO) và ancol đa chức (vì cấu trúc phân tử có tới 5 nhóm -OH ở vị trí liền nhau)
a) Glucose mang các tính chất của ancol đa chức
+) Glucose tác dụng với Cu(OH)2 với điều kiện ở nhiệt độ thường. Dung dịch glucose hòa tan được Cu(OH)2 tạo ra dung dịch có màu xanh lam là phức đồng – glucose
2 C6H12O6 + Cu(OH)2 → (C6H11O6)2Cu + 2 H2O
+) Glucose tham gia phản ứng tạo este
C6H7O(OH)5 + 5 (CH3CO)2O → C6H7O(OOCCH3)5 + 5 CH3COOH
b) Glucozo có tính chất của anđehit
+) Phản ứng Oxy hóa glucose
• Glucose + AgNO3
Glucose tác dụng với dung dịch AgNO3 trong NH3, điều kiện đun nóng (thuốc thử Tollens) cho ra phản ứng tráng bạc:
CH2OH[CHOH]4CHO + 2 Ag(NH3)2OH → CH2OH[CHOH]4COONH4 + 2 Ag + 3 NH3 + H2O
Trong đó CH2OH[CHOH]4COONH4 là amoni gluconat
• Glucose + NaOH + Cu(OH)2
Glucose tác dụng với dung dịch Cu(OH)2 trong NaOH, dưới điều kiện đun nóng (thuốc thử Felinh) tạo thành Cu2O tạo thành kết tủa có màu đỏ gạch.
CH2OH[CHOH]4CHO + NaOH + 2 Cu(OH)2 → CH2OH[CHOH]4COONa + Cu2O (đỏ gạch) + 3 H2O
Trong đó CH2OH[CHOH]4COONa là Natri gluconat
• Glucose làm mất màu nước Brom (Glucose + Br2)
CH2OH[CHOH]4CHO + Br2 + H2O → CH2OH[CHOH]4COOH + 2 HBr
+) Phản ứng khử glucose bằng Hidro.
• Glucozo + H2
– Khi dẫn khí H2 vào trong dung dịch glucose được đun nóng (với xúc tác Ni), thu được một polyancol được biết đến là sobitol:
CH2OH[CHOH]4CHO + H2 → CH2OH[CHOH]4CH2OH
c) Phản ứng lên men của Glucose
– Khi có mặt enzym xúc tác ở nhiệt độ trong khoảng 30 – 35°C, glucose sẽ bị lên men và tạo ra sản phẩm là ancol etylic (C2H5OH) và khí cacbonic (CO2)
C6H12O6 → 2 C2H5OH + 2 CO2
Đăng ký ngay để được các thầy cô ôn tập kiến thức và xây dựng lộ trình ôn thi THPT sớm ngay từ bây giờ

4. Công thức hóa học của đường Fructose
4.1. Công thức hóa học của đường Fructose là gì?
Fructose, hay còn thường gọi là đường fructô, đường trái cây hay đường hoa quả, bản chất là một monosaccharide ketonic đơn giản tìm thấy trong khá nhiều loài thực vật, đó là nơi mà nó thường được liên kết với glucose để hình thành những disaccharide sucrose.
Đường Fructose thường tồn tại dưới 2 dạng:
+ Dạng thứ nhất là đường fructose tự nhiên, thường được tìm thấy được trong mật ong, các loại quả như táo, chà là hoặc nước ép trái cây nguyên chất và một lượng nhỏ chứa trong rau củ như ở trong cà rốt.
+ Dạng thứ hai là đường fructose tinh luyện thường góp mặt trong các loại thực phẩm như kẹo, sữa chua có đường, soda, hoa quả đóng hộp, nước ép, kem.
-
Công thức phân tử đường fructose là C6H12O6

-
Cấu tạo của Fructose khá giống với đường Glucose, nó cũng có khả năng chuyển hóa giữa mạch vòng và mạch thẳng
-
Fructose cũng chứa nhóm OH hemiaxetal – nhóm OH được gắn màu ở vị trí C2, do đó mà nhóm OH này cũng mang những tính chất giống như đường Glucose
-
Sự khác nhau giữa chúng chính là vị trí của nhóm C=O hình thành nên sự đóng vòng của đường fructose là 1 vòng với 5 cạnh
-
Có thể nhận thấy rõ ràng là fructose và glucose có công thức phân tử tương tự nhau, chỉ khác nhau ở công thức cấu tạo – chúng là đồng phân với nhau, do vậy mà 2 hợp chất này có khả năng chuyển hóa qua lại cho nhau nếu đặt trong điều kiện thuận lợi
-
Từ đó, có thể nhận thấy mặc dù không có nhóm -CHO nhưng fructose vẫn có khả năng tham gia phản ứng tráng gương, đó là do trong môi trường bazơ NH3, fructose có khả năng chuyển hóa thành glucose.
-
Glucose và fructose đều có những tính chất hóa học hoàn toàn giống nhau khi trong cùng 1 môi trường kiềm.
Dưới đây là một số thông tin khác về đường Fructose dành cho các em tham khảo:
• Tên đặt theo hệ thống của đường fructose là: 1, 3, 4, 5, 6-Pentahydroxy-2-hexanone
• Tên khác của đường fructose là fruit sugar, levulose, D-fructofuranose, D-fructose, D-arabino-hexulose
• Danh pháp IUPAC của đường fructose là 1, 3, 4, 5, 6-Pentahydroxy-2-hexanone
• Khối lượng riêng của đường fructose là 1.694 g/cm3
4.2. Tính chất hóa học của đường Fructose
– Vì phân tử fructozơ bao gồm 5 nhóm OH, trong đó có 4 nhóm liên tiếp liền kề và chứa 1 nhóm chức C=O nên nó có những tính chất hóa học của ancol đa chức và của cả xeton nữa.
– Ở nhiệt độ bình thường, có thể hòa tan Cu(OH)2..
– Có xảy ra phản ứng với anhiđrit axit để hình thành nên este 5 chức.
– Chúng có những tính chất của xeton
+ Phản ứng với H2 tạo sobitol.
+ Tác dụng được với HCN (axit xiahidric)
– Trong môi trường kiềm, fructozơ có khả năng chuyển hóa thành glucozơ nên fructose cũng có phản ứng tráng gương và tác dụng với
Cu(OH)2 trong điều kiện môi trường kiềm.
Fructozo ⇄ Glucozo
– Fructose không tham gia được phản ứng làm mất màu của dung dịch Brom.
* Chú ý: Không phân biệt 2 loại đường glucose và fructose bằng phản ứng tráng bạc hay tác dụng với Cu(OH)2 trong môi trường kiềm khi đun nóng vì nó có thể chuyển hóa thành nhau. Để phân biệt glucose với fructose thì phải dùng đến phản ứng với dung dịch nước brom.
Trong video clip dưới đây, cô Kim Oanh sẽ hệ thống toàn bộ nguồn gốc, cấu tạo, tính chất vật lí, tính chất hóa học của Glucozo và Fructozo; Saccarozơ và Mantozơ trong nhóm Cacbohidrat. Cùng cô theo dõi bài giảng để tiếp thu kiến thức hiệu quả nhất các em nhé!
Công thức hóa học của đường là một phần kiến thức tuy nhỏ nhưng rất quan trọng đối với các em học sinh. Bởi vậy VUIHOC tổng hợp bài viết này để các em ôn tập dễ dàng hơn. Để tìm hiểu về các chất hữu cơ khác cũng như kiến thức về môn Hoá học THPT, các em truy cập vào Vuihoc.vn để đăng ký tài khoản hoặc liên hệ trung tâm hỗ trợ ngay để học hỏi thêm thật nhiều kiến thức nhé!
